 首页 /
新闻
首页 /
新闻
 2025-04-26
2025-04-26最新研究表明人脐带间质干细胞来源的外泌体与水凝胶联合构建的给药系统exo@H可以有效的缓解实验性牙周炎小鼠的炎症反应和组织损伤。牙周炎(periodontitis)是一种发生在牙周组织的慢性炎症性破坏性疾病,是目前导致成人牙齿缺失的首要原因。
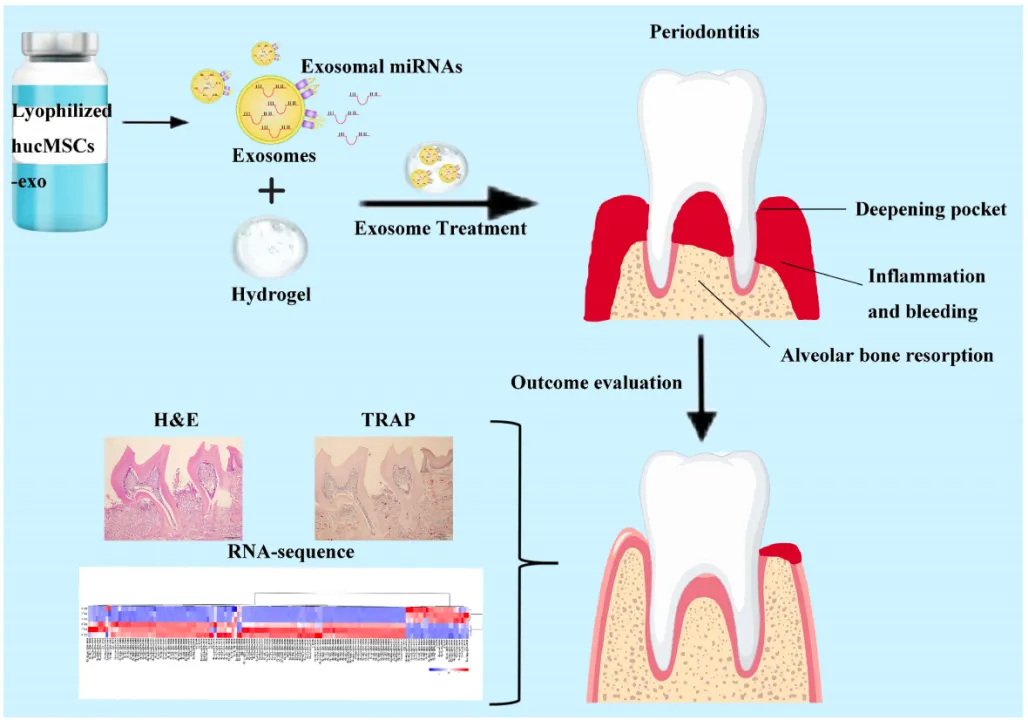
该研究使用具有高生物相容性,良好生物降解性和亲水性的水凝胶与冻干的hucMSCs-exo(人源脐带间质干细胞外泌体)相融合,制备了可用于牙周炎治疗的给药系统 exo@H。
通过体外实验证明外泌体的有效性和最适剂量
体外建立LPS诱导的MC3T3-E1细胞(小鼠胚胎成骨细胞前体细胞)炎症模型,分别进行水凝胶(Hydrogel)、外泌体(exo)、exo@H等处理发现exo@H对于提高MC3T3-E1细胞的活性有着显著的促进作用,ALP和ARS染色试验证明了exo@H可以促进细胞的成骨分化和钙沉积。
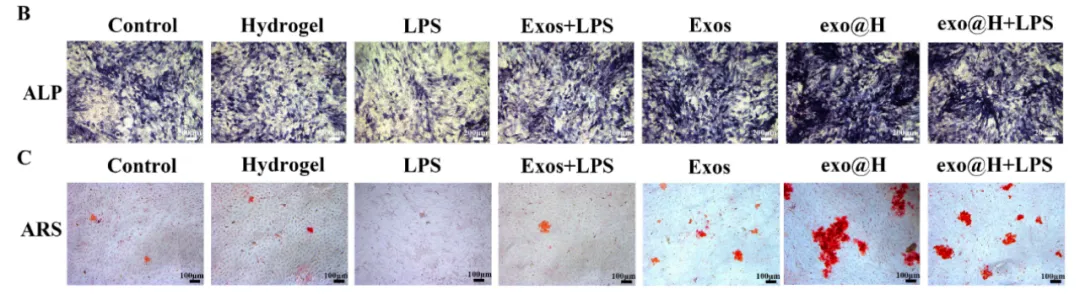
研究人员检测了在不同浓度外泌体条件下的MC3T3-E1细胞的活性,结果表明细胞活性随着外泌体浓度的增高而显著地增加,但施加的浓度达到一定临界浓度后细胞活性开始下降,这表明外泌体在促进MC3T3-E1细胞分化中具有一定的临界阈值,并证明了外泌体的最适浓度为1×109 (particles/mL) 。
验证Exo@H在小鼠牙周炎动物模型(Ligature-Induced Periodontal Model)中的作用
小鼠牙周炎模型所用小鼠,动物随机分4组:
1:假手术组;
2:模型组;
3:水凝胶组
4:exo@H组
该动物模型首先测量了ABC-CEJ的距离(ABC-CEJ指标有助于评估牙槽骨的吸收程度,据此判断牙周炎疾病的进程),结果发现Exo@H能够显著地缓解和治疗实验小鼠的牙周炎,并用HE染色和Trap染色实验加以证明。
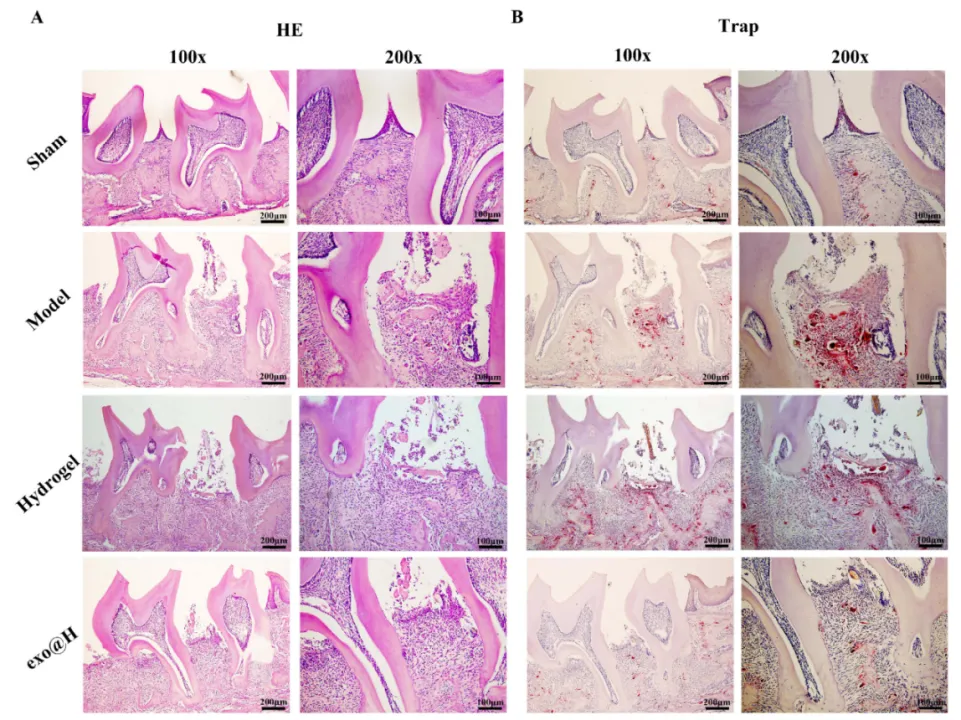
exo@H对组织的miRNA转录组分析
该研究提取了各组小鼠牙龈组织的总RNA并完成了对该组织的miRNA测序及后续分析。
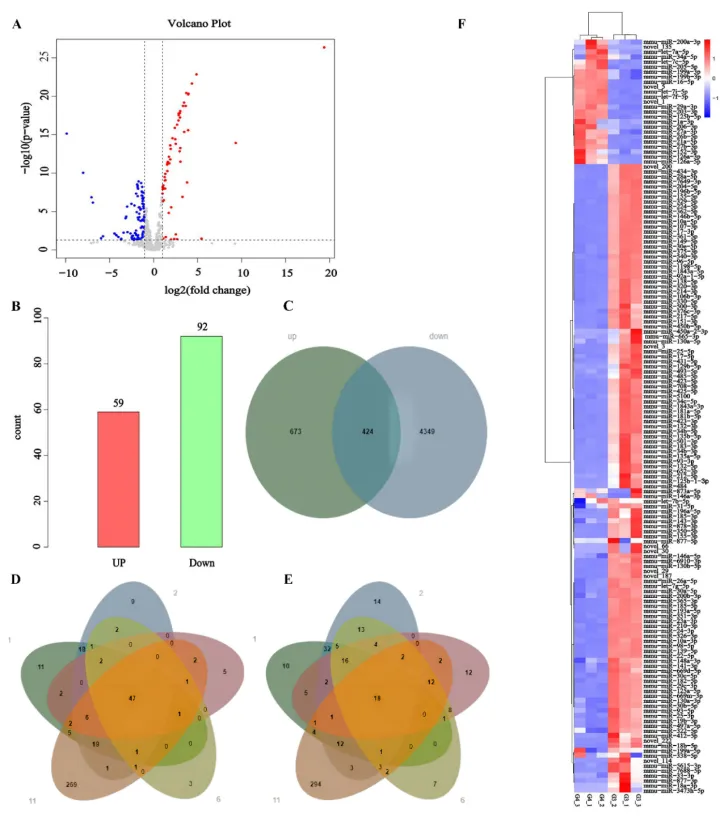
与水凝胶组相比,exo@H处理组分别筛选出了59个表达上调的miRNA基因以及92个表达下调的miRNA基因。通过对得到的差异表达miRNA基因的功能富集分析(GO functional analysis)和KEGG通路分析发现了与炎症响应有关的信号通路,例如:Notch signaling pathway 和MAPK signaling pathway 等。
该论文研究人员最后通过qRT-PCR、WB以及荧光素酶报告实验等验证了2个差异表达miRNA : let-7f-5p和miR-203-3p,以及它们分别对应的靶基因IL-13和Nit2。let-7f-5p可以促进骨组织细胞的形成,其靶基因IL-13具有抗炎等作用,而miR-203-3p的靶基因Nit2可以通过氮硫代谢途径参与细胞的生长以及维持细胞的自我平衡。
本文亮点
本研究通过miRNA测序探究了exo@H药物对牙龈组织miRNA表达谱的影响,并鉴定了两个可能与炎症反应等信号通路有关的miRNA(let-7f-5p和miR-203-3p)及其对应的靶基因(IL-13和Nit2),为后续的分子机制研究奠定基础。
可深入的验证实验
1,该研究在进行miRNA测序的同时,还可以对相同组织进行RNAseq和蛋白质组学研究,以了解exo@H对目标治疗组织在多组学水平上的影响,这样经过后续的生物信息学分析流程可能得到与外泌体治疗牙周炎相关的调控通路。
2,本研究证明了在exo@H药物治疗牙周炎过程中有两个miRNA及其靶基因表达量被显著上调,接下来的试验是否可以考虑在细胞中分别过表达这两个miRNA或其靶基因,进而观察与骨细胞活性有关的表型和指标,同理,也可以对这两个靶基因进行敲低试验去观察细胞表型。
论文原文及链接:
Human Umbilical Cord Mesenchymal Stem Cells-Derived Exosomes Attenuates Experimental Periodontitis in Mice Partly by Delivering miRNAs.
https://doi.org/10.2147/IJN.S502192
期刊简介:International Journal of Nanomedicine,中科院医学2区,IF6.7
通讯作者简介:王琳源,主任医师,锦州医科大学附属口腔医院牙周黏膜科主任,牙周微创中心主任,口腔内科教研室主任,口腔临床医学博士,硕士研究生导师
编者简介:张博森, 清华大学生物学博士,美国UIUC博士后研究员,现为沈阳盛京生物细胞研发中心有限公司实验室主任。
外泌体冻干粉制备:沈阳盛京生物细胞研发中心有限公司